[⁶⁸Ga]Ga-OncoACP3-DOTA PET 首批人體試驗結果解析
作者: 黃玉儀 醫師(和信治癌中心醫院 核子醫學科)
前言:PSMA 之外,還有誰?
過去十年,PSMA(攝護腺特異膜抗原)標靶診療已徹底翻轉晚期攝護腺癌的治療版圖——從 [⁶⁸Ga]Ga-PSMA-11 的精準影像偵測,到 [¹⁷⁷Lu]Lu-PSMA-617(Pluvicto®)的放射性核種治療,PSMA 儼然成為攝護腺癌核醫診療標靶的代名詞。
然而,PSMA 並非萬能:約 10–15% 的轉移性去勢抵抗性攝護腺癌(mCRPC)患者為 PSMA 低表現或陰性,對現有放射性藥物療法(RPT)完全無法受益。即使 PSMA 表現充足,唾液腺與腎臟的「非腫瘤攝取」也持續困擾著α粒子治療的劑量安全窗。
正是在此背景下,一個沉寂多年的老牌生物標記悄悄重返舞台——ACP3(攝護腺酸性磷酸酶,Prostatic Acid Phosphatase),並以嶄新的放射性配體身份,在 2025 年 SNMMI 年會亮相,震撼核醫學界。
ACP3 是什麼?為何值得關注?
ACP3(Acid Phosphatase 3)早在 1936 年即被發現是攝護腺癌的血清標記(早於 PSA 問世數十年),曾是診斷攝護腺癌的主力指標。然而隨著 PSA 普及,ACP3 逐漸淡出臨床視野。
但作為診療標靶,ACP3 具備幾項關鍵優勢:
| 特性 | ACP3 | PSMA |
|---|---|---|
| 攝護腺癌表現率 | >95% 的攝護腺癌 | 高,但有 10–15% 低/陰性 |
| 腫瘤表現量 | 平均高於 PSMA | 高 |
| 唾液腺攝取 | 極低 | 明顯(限制α療法安全性) |
| 腎臟攝取 | 極低 | 中至高 |
| 正常器官整體背景 | 更乾淨 | 較多非腫瘤攝取 |
簡言之,ACP3 的腫瘤表現量比 PSMA 更豐富,而正常組織的「雜訊」卻更少——這正是核醫診療標靶的理想組合。
配體開發:從 DNA 編碼化學庫到臨床
傳統藥物篩選費時費力。瑞士 Philochem AG(Philogen SpA 子公司)採用**DNA 編碼小分子化合物庫(DNA-encoded chemical library, DEL)**技術,從數億種化合物中快速篩選出對 ACP3 具超高親和力的小分子配體——OncoACP3-DOTA。
這項成果於 2024 年發表於 Journal of Nuclear Medicine(Cazzamalli et al., J Nucl Med 2024;65:241120),確認其體外與活體動物模型的優異表現。隨後,德國明斯特大學依德國藥事法(AMG)第 13.2b 條取得製造與使用許可,完成從實驗室到人體的關鍵跨越。
SNMMI 2025 首批人體影像結果
研究設計
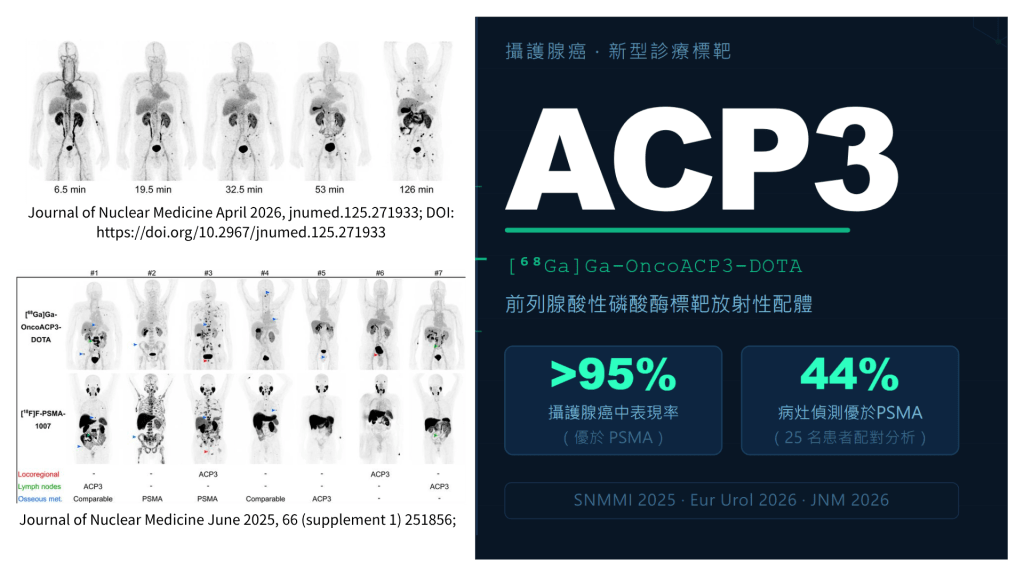
2025 年 6 月,SNMMI 年會於美國紐奧良舉行。德國明斯特大學核醫學科 Dr. Philipp Backhaus 發表了迄今最完整的 [⁶⁸Ga]Ga-OncoACP3-DOTA PET 人體初步成果,納入首批接受掃描的 25 名攝護腺癌患者,並與 [¹⁸F]PSMA-1007 進行頭對頭比較(23 名有配對 PSMA 掃描,共 27 對配對掃描)。
主要發現
1. 正常器官背景更乾淨
[⁶⁸Ga]Ga-OncoACP3-DOTA 在唾液腺與腎臟的攝取顯著低於 [¹⁸F]PSMA-1007(p < 0.002),這對未來搭配α粒子核種(如 ²²⁵Ac)的治療應用意義重大——唾液腺毒性長期以來是 ²²⁵Ac-PSMA α療法的主要限制因素。
2. 腫瘤偵測能力不遜於 PSMA
整體而言,兩者在局部或轉移性攝護腺癌病灶的 SUVmax 無顯著差異。在 25 對配對分析中,11 對(44%)ACP3 表現更佳,8 對(32%)PSMA 更佳,其餘相當。
在淋巴結轉移患者中,ACP3 甚至偵測到更多淋巴結病灶(分別為 10 vs 7 顆、14 vs 8 顆),且 SUVmax 更高(36.7 vs 13.9)。
3. 改變臨床決策
這或許是最具說服力的臨床意義指標:
- 7/25 名患者(28%)的診斷評估因 ACP3 PET 結果而改變
- 9/25 名患者(36%)的治療計畫因此調整
具體而言,在 6 名生化復發患者中,ACP3 PET 改變了 3 名(50%)的治療方向;在 12 名已知轉移患者中改變了 2 名(17%)的處置。
研究局限
Dr. Backhaus 坦承幾項重要限制:
- 回顧性設計,兩次掃描並非同步進行(ACP3 PET 平均晚 16 天,可能有利於 ACP3 偵測更多病灶)
- 樣本數仍小
- 尚無治療部分的人體安全性與療效資料
2025–2026 年最新進展
① European Urology 全文論文(2026)
SNMMI 的初步資料已正式發表於泌尿外科頂尖期刊European Urology:Translational and first-in-human positron emission tomography targeting prostatic acid phosphatase in prostate cancer using the ligand [⁶⁸Ga]Ga-OncoACP3-DOTA.
論文結論指出,OncoACP3-DOTA 強烈的腫瘤攝取加上低器官背景,為未來正式的 PET 影像與放射性核種治療試驗提供堅實基礎。
② JNM 藥動學與放射劑量學論文(2026 年 4 月,最新刊出)
Journal of Nuclear Medicine 於 2026 年 4 月剛發表第一份針對 mCRPC 患者的 [⁶⁸Ga]Ga-OncoACP3-DOTA 藥動學與放射劑量學分析(Brosch-Lenz et al., JNM 2026),系統性評估其在人體的藥物分布動力學,是邁向治療性核種標記(如 [¹⁷⁷Lu] 或 [²²⁵Ac])的必要前置工作。
③ RayzeBio(BMS)將其納入臨床前管線
Bristol Myers Squibb 旗下放射性藥物平台公司 RayzeBio 已將 OncoACP3 的治療版本重新命名為:
- RYZ701(治療用)
- RYZ711(診斷用)
目前正積極推進臨床前開發,尤其鎖定PSMA 低/陰性患者這個迫切的未滿足醫療需求族群。
④ European Urology 綜述「路線圖」(2026 年 1 月)
歐洲泌尿科學雜誌刊出專題綜述《Targeting Prostatic Acid Phosphatase in Prostate Cancer: Roadmap on How To Venture Above and Beyond PSMA with ACP3 Theranostics》,正式為 ACP3 診療標靶在臨床轉譯中的角色定位,並規劃出未來臨床試驗的發展路線圖。
與 PSMA 的關係:競爭?還是互補?
ACP3 並非要「取代」PSMA,從Dr. Backhaus發表論文中的少量影像來評估,ACP3在骨骼轉移病灶的表現量是否能達成與PSMA一致或更好仍有待商榷,還需要更多的研究比較驗證,因而,現今看來ACP3與PSMA應為形成策略性互補的角色:
PSMA 高表現患者 → PSMA-PET / Lu-177 PSMA-617(現有標準)PSMA 低/陰性患者 → ACP3-PET / RYZ701(新興選擇)PSMA 陽性但α療法候選者 → ACP3(唾液腺安全性更佳)不確定病灶 → ACP3 + PSMA 雙軌影像,提升偵測率
此外,ACP3 的超低唾液腺攝取,使其成為α粒子核種(²²⁵Ac)放射性配體治療的理想搭配標靶,而α粒子的高LET特性,也許能降低APC3在PET影像上的治療需求攝取值門檻——這可能是 ACP3 診療標靶最具臨床革命性的應用場景。
台灣觀點
對台灣核醫診療標靶領域而言,ACP3 的發展有幾層意義:
- 攝護腺癌是台灣男性常見癌症,隨著 [¹⁷⁷Lu]Lu-PSMA 治療逐步推展,PSMA 陰性族群的替代方案需求將日益迫切
- α粒子核種的引進(如 ²²⁵Ac-PSMA)在仍面臨治療唾液線毒性的挑戰,ACP3 的低唾液腺毒性優勢可能降低這一障礙
- 國際臨床試驗接軌:ACP3 正式臨床試驗即將展開,台灣核醫中心宜密切關注,爭取早期進入試驗機會
結語
[⁶⁸Ga]Ga-OncoACP3-DOTA 的人體首批結果,讓攝護腺癌診療標靶的未來更加令人期待。一個被遺忘 40 年的老牌標記,因核醫診療標靶技術的成熟而重獲新生——這正是轉譯醫學的魅力所在。
從 DEL 化合物庫的基礎發現,到 SNMMI 的首批人體影像,再到 European Urology 的正式發表、BMS/RayzeBio 的產業進入,ACP3 正以驚人速度走完從實驗室到臨床的路。
我們將持續追蹤 RYZ701/RYZ711 的臨床試驗進展,歡迎關注本協會網站最新資訊。
參考文獻
- Cazzamalli S, et al. First-in-class ACP3 ligand from DNA-encoded chemical library. J Nucl Med 2024;65:241120.
- Backhaus P, et al. Translational and first-in-human PET targeting ACP3 using [⁶⁸Ga]Ga-OncoACP3-DOTA. Eur Urol 2026;89:305–310.
- Brosch-Lenz J, et al. Dynamics, pharmacokinetics, and dosimetry of first-in-human [⁶⁸Ga]Ga-OncoACP3-DOTA PET in mCRPC. J Nucl Med 2026 Apr (Epub ahead of print). DOI: 10.2967/jnumed.125.271933.
- Targeting Prostatic Acid Phosphatase in Prostate Cancer: Roadmap on How To Venture Above and Beyond PSMA with ACP3 Theranostics. Eur Urol 2026 (Review).
- The prostatic acid phosphatase in prostate cancer: A novel theranostic target. ScienceDirect 2026.
- RayzeBio. ACP3 pipeline (RYZ701/RYZ711). rayzebio.com/pipeline/acp3/ (accessed May 2026).
- Philogen SpA. OncoACP3 imaging & therapy pipeline. philogen.com (accessed May 2026).
本文本文撰寫過程採用 AI 協作方式完成:以Claude進行文獻搜尋建議與初步撰稿,並由作者進行專業審閱與最終確認。由台灣核醫診療標靶治療之友協會編輯整理,資訊截至 2026 年 5 月。本文為衛教資訊,不構成個人醫療建議。如有相關診療需求,請諮詢您的主治醫師。